GPIIIa gēns (3.A
att.) atrodas 17. hromosomā, ir 46 kb
liels un satur 14 eksonus (Zimrin et al. 1990). Tas kodē 788
aminoskābju garu
proteīnu, kas papildus nobrieduša GPIIIa aminoskābju secībai ietver arī
26
aminoskābju signālpeptīdu.
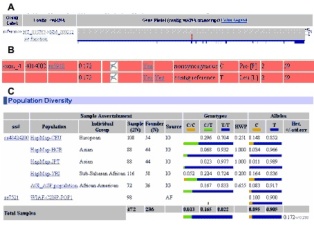
3. attēls. GPIIIa gēns (A), PlA1/A2
polimorfisms (B) un tā alēļu frekvences dažās populācijās (C) (http://www.ncbi.nlm.nih.gov/SNP/snp_ref.cgi?rs=5918).
Figure 3. GPIIIa
gene (A), PlA1/A2 polymorphism (B) and its allele
frequencies in some populations (C) (http://www.ncbi.nlm.nih.gov/SNP/snp_ref.cgi?rs=5918).
GPIIIa
gēnam zināmas vairākas ģenētiskās variācijas
eksonos un daudzas intronos, taču vienīgais polimorfisms, kas,
iespējams,
saistīts ar arteriālās trombozes un miokarda infarkta risku ir PlA1/A2.
Šis polimorfisms ir T/C variācija 4. eksonā (Newman et al. 1988; 3.A,B
att.),
kura izraisa 59. leicīna apmaiņu pret prolīnu (nobriedušā GPIIIa tas
atbilst
33. pozīcijai). Kaut arī dotā apmaiņa neatrodas receptora ligandu
saistības
rajonā, in vitro ir parādīts, ka tā
izmaina fibrinogēna receptora konformāciju un ietekmē funkcionālo
aktivitāti.
Dati liecina, ka PlA2 variantam raksturīgs zemāks
ADF-atkarīgās
trombocītu aktivācijas slieksnis, pastiprināta fibrinogēna, saistīšana,
pastiprināta trombocītu agregācija un tromba veidošanās, t.i.,
paaugstināts
trombozes ‘potenciāls’ (Byzova and Plow 2000). Ir veikta arī virkne
asociācijas
analīžu par PlA1/a2 polimorfisma saistību ar trombozes un
MI risku.
Kaut arī rezultāti ir pretrunīgi, tomēr vairums datu skaidri norāda uz
PlA2
alēles protrombotisko fenotipu un saistību ar paaugstinātu miokarda
infarkta
risku. Ir norādes arī par polimorfisma farmakoģenētisko nozīmi
attiecībā uz
antitrombotiskajiem līdzekļiem (Mikkelsson et al. 2005).